Tratamiento Farmacológico De La Hepatitis C Crónica, Genotipo 1
Nota del autor
- Este texto no es en ningún caso una guía terapéutica ni farmacológica para el VHC crónica.
- El objetivo es que el lector conozca la dimensión sanitaria de la hepatitis C crónica, sus complicaciones y los tratamientos utilizados en un contexto actual de novedades diarias.
La hepatitis C fue reconocida por primera vez a principios de la década de 1970, cuando se generalizó la disponibilidad de pruebas serológicas para los virus de la hepatitis A y B. La mayoría de los casos de hepatitis asociadas a transfusiones no eran producidas por ninguno de estos virus, y así surgió la denominación de hepatitis no A no B.
A finales de la década de 1980 se identificó un antígeno asociado con la hepatitis no A no B y se denominó virus de la hepatitis C (VHC).
El VHC tiene una gran variabilidad genética, de tal forma que existen 6 genotipos numerados del 1 al 6 y múltiples subtipos. En Europa el genotipo 1 es el más frecuente, aunque su prevalencia puede variar de un país a otro. En España la prevalencia aproximada de los diferentes genotipos es la siguiente: 75% el genotipo 1b; 10% el 1a; 5% el 3; 3% el 2; 2% el 4; 0.5% el 5; cerca del 0% el 6; y 4.5% el 1 asociado a otros genotipos. Por tanto, el genotipo 1 es el más frecuente en nuestro país y, desafortunadamente, este es el genotipo con menor tasa de respuesta al tratamiento (50% del genotipo 1 frente al 80% del genotipo 2 y 3).
Esto es lo que sucedía hasta hace muy poco con el mejor tratamiento del que se disponía
Prevalencia De La Infección Por VHC
La infección crónica por VHC afecta aproximadamente al 3% de la población mundial. Actualmente es la causa del 70% de las hepatitis crónicas, el 40% de las cirrosis hepáticas, el 60% de los hepatocarcinomas, y el 30% de los trasplantes hepáticos. En otras palabras, el VHC es actualmente la primera causa de hepatitis crónica, cirrosis hepática, hepatocarcinoma y trasplante hepático.
En Europa se ha calculado que existen más de 5 millones de pacientes infectados, aunque la prevalencia no es uniforme variando desde el 0.5% en los países del norte al 2% en los países mediterráneos. La distribución de la infección por grupos de edad muestra un pico de máxima seroprevalencia en el grupo de 30-39 anos y después un progresivo incremento con la edad.
La elevada frecuencia y la potencial morbi-mortalidad convierten a la infección crónica por VHC en un problema mayor de salud pública.
La hepatitis aguda por VHC
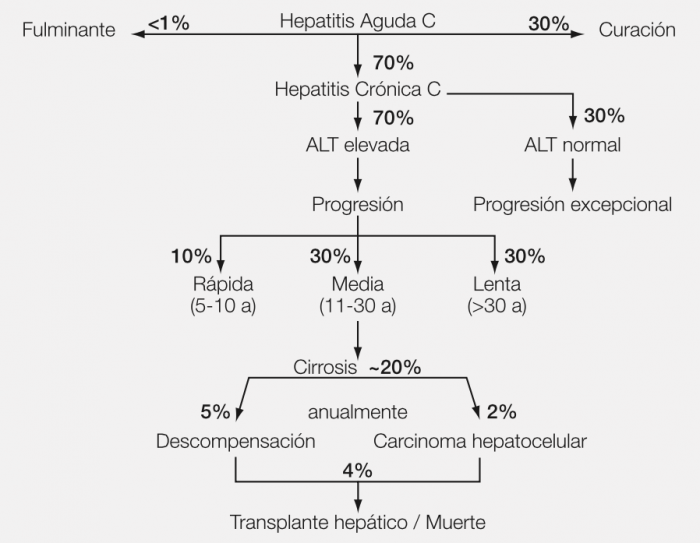
Suele tener un curso subclínico, por lo que se diagnostica muy pocas veces. Su característica más importante es su elevada tendencia a evolucionar a la cronicidad: 70% de los casos. De los pacientes con infección crónica por VHC, el 70% presentan una elevación mantenida de las transaminasas (hepatitis crónica habitual), mientras que en el 30% restante el nivel sérico de transaminasas es normal (hepatitis crónica con transaminasas normales).
Fases de la hepatitis C
Fase 1: Infección aguda (Los primeros seis meses)
Cuando la hepatitis C entra en el torrente sanguíneo llega al hígado. El virus infecta las células del hígado y comienza a crecer. Alrededor del 20% de las personas pueden eliminar el virus por sí solas en unos meses.
Fase 2: Infección crónica
Alrededor del 80% de la gente no puede eliminar el virus por su cuenta y desarrollará una infección a largo plazo.
Fase 3: Inflamación y fibrosis
El virus se multiplica matando las células del hígado y este daño conduce a la inflamación hepática. Con el tiempo, este daño lleva a crear cicatrices en el hígado, llamada fibrosis. El virus actúa lentamente, muchas veces tomando más de 20 o 30 años, y la persona puede no demostrar ningún síntoma.
Fase 4: Cirrosis
Durante los 20 a 30 años de una infección crónica, una de cada cinco personas puede desarrollar una cicatrización más severa y un endurecimiento del hígado llamado cirrosis. El hígado de algunas personas seguirá funcionando normalmente y no demostrará síntomas. Para otras personas la cirrosis puede comenzar a afectar las funciones normales del hígado. La cicatrización generalizada hace que el hígado se encoja y existe el riesgo de insuficiencia hepática. En este punto, se puede considerar un trasplante de hígado. Entre el cinco y el diez por ciento de las personas con cirrosis desarrollarán cáncer del hígado.
La cirrosis hepática
Constituye el punto crítico de la hepatitis crónica por VHC, ya que a partir de ese momento existe riesgo de morbilidad (descompensación o desarrollo de hepatocarcinoma) y de mortalidad secundaria. En la hepatitis crónica con transaminasas elevadas la lesión hepática progresa a cirrosis hepática con mucha mayor frecuencia. La tasa de progresión puede ser rápida (5-10 años), media (11-30 años) o lenta (>30 años), de tal forma que finalmente alcanzan el estadio de cirrosis aproximadamente un 20% de los pacientes. Los factores de riesgo para progresar a cirrosis son virológicos (coinfección por virus B o VIH), histológicos (lesión hepática intensa en la biopsia diagnóstica, hepatopatía grasa asociada) o del huésped (edad superior a 40 años en el contagio, sexo masculino, ingesta tóxica de alcohol, síndrome metabólico). Los estudios de seguimiento de hasta 10 años de los enfermos con cirrosis compensada han revelado que anualmente un 5% presentan descompensaciones hepáticas (ascitis, hemorragia digestiva, encefalopatía, infecciones), un 2% desarrollan hepatocarcinoma, y un 4% mueren por estas causas a menos que se practique un trasplante hepático.
El tratamiento de la hepatitis crónica por VHC
Independientemente del tratamiento a seguir el objetivo es conseguir la denominada Respuesta Virológica Sostenida (RVS). Esta se define como la persistencia del ARN del VHC negativo a los 6 meses de haber finalizado el tratamiento.
Tradicionalmente el tratamiento consistía en la combinación de interferón pegilado (PEG-IFNα) más ribavirina (RBV), con una respuesta RVS global del 55% (>40% en genotipos 1 y 4, > 80% en genotipos 2 y 3). Se observa mejoría histológica en cerca del 75% de los pacientes que reciben este tratamiento.
Cerca del 90% de las respuestas virológicas se observan en las primeras 12 semanas del tratamiento y luego son ocasionales. La mayor parte de las recurrencias surgen en las 12 semanas siguientes del tratamiento. Si el tratamiento resulta exitoso la RVS es duradera llegando a corroborarlo una década después del tratamiento.
La variabilidad en el éxito del tratamiento con interferón se correlaciona con:
- Genotipo favorable (genotipos 2 y 3 a diferencia de los genotipos 1 y 4).
- Cifra basal baja de RNA del HCV < 2 millones de copias/ml
- Hepatitis leve por los datos histológicos.
- Fibrosis mínima.
- Tener < 40 años.
- No ser obeso ni presentar resistencia a la insulina ni DM II
- Ser mujer.
En personas con el genotipo 1 el tratamiento debe durar 48 semanas completas, los que tienen los genotipos 2 y 3 basta con un ciclo de 24 semanas.
El interferón pegilado (peginterferón o PEG IFN) se inyecta una vez por semana de forma subcutánea y la ribavirina se toma todos los días repartiendo la dosis total diaria en dos tomas coincidiendo con la ingesta de alimentos, no morder ni partir.
Existen dos tipos de interferones pegilados α-2b y α-2a, en base a su tamaño y volumen de distribución PEG IFN α2a se administra con una dosis uniforme sin importar el peso de la persona, mientras que PEG IFN α2b debe basarse en el peso del paciente, (1,5mcg/kg/sem).
En el último año ha habido una revolución en el tratamiento de la hepatitis C. Me centraré en el tratamiento farmacológico para el VHC crónica del genotipo 1 autorizados en España desde Marzo del 2014.
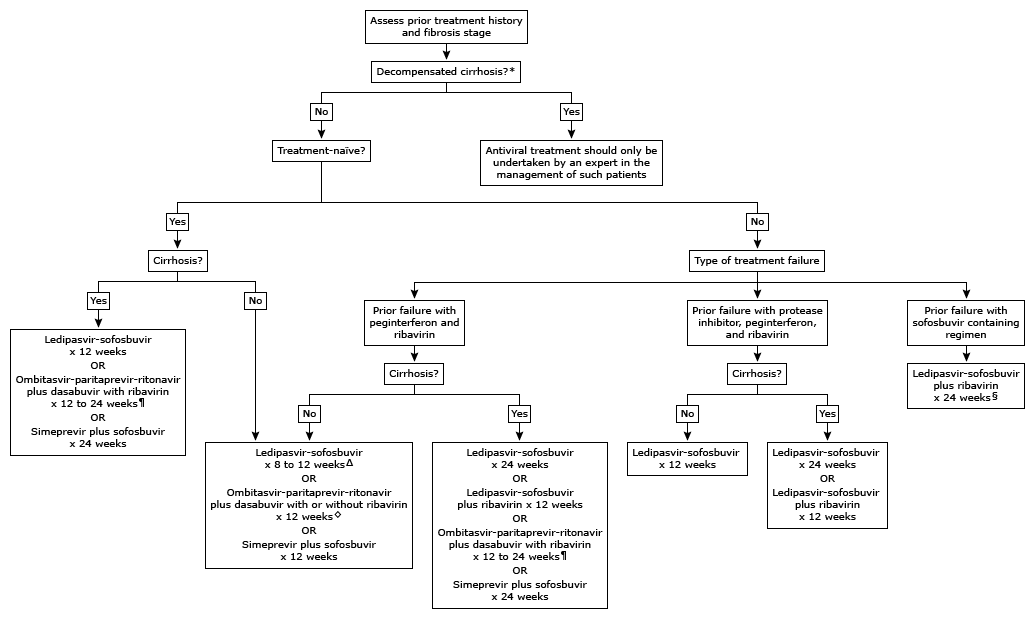
En el siguiente algoritmo podemos ver cuales son los tratamientos recomendados a fecha 29/1/2015.
Los fármacos son los siguientes:
- Harvoni® sus principios activos son ledipasvir + sofosbuvir, autorizado en España desde 15/12/2014 y a día de hoy no comercializado.
- Viekirax® sus principios activos son ombitasvir + paritaprevir + ritonavir, autorizado en España desde 3/2/2015 y a día de hoy no comercializado.
- Exviera® su principio activo es dasabuvir, autorizado en España desde 3/2/2015 y a día de hoy no comercializado.
- Olysio® su principio activo es simeprevir, autorizado en España desde 3/6/2014 y comercializado.
- Sovaldi® su principio activo es sofosbuvir, autorizado en España desde 5/03/2014 y comercializado.
Estos tratamientos coinciden en no utilizar interferón, entre todos ellos destaca Harvoni®, su administración es una única pastilla diaria.
El 26/02/2015 el Ministerio de Sanidad, Servicios sociales e Igualdad ha emitido una nota de prensa con el título “Los pacientes de hepatitis C serán tratados con los nuevos medicamentos de acuerdo con los criterios del Plan Estratégico” dicha nota de prensa explica las conclusiones del comité de expertos entre las que destaca la necesidad de emplear los nuevos antivirales contra esta enfermedad, que simplifican el tratamiento, reducen las necesidades de seguimiento, aumentan las tasas de curación y retrasa la aparición de complicaciones, para un amplio grupo de pacientes. En concreto, aconsejan tratar con distintas combinaciones, según el genotipo, a todos los pacientes con fibrosis en grado F2, F3 y F4.
Los pacientes prioritarios son los siguientes:
- Pacientes con fibrosis hepática significativa (F2 a F4) con independencia de la existencia o no de complicaciones previas a la hepatopatía.
- Pacientes en lista de espera de trasplante hepático o trasplantados (hepáticos que hayan vuelto a infectarse y no hepáticos con hepatitis C).
- Pacientes que no hayan respondido a la triple terapia con inhibidores de la proteasa de primera generación.
- Pacientes con hepatitis C con manifestaciones extrahepáticas clínicamente relevantes del virus de la hepatitis C, sea cual sea el grado de fibrosis.
- En cualquier caso, y también con independencia del grado de fibrosis, se debe indicar el tratamiento en pacientes con elevado riesgo de trasmisión y mujeres en edad fértil que deseen un embarazo.
En la Comisión Interministerial de Precios de los Medicamentos celebrada el pasado lunes, 23/2/2015, se ha acordado incorporar tres nuevos medicamentos, Harvoni® (una combinación de sofosbuvir más ledipasvir) y Vikerax® y Exviera® (una combinación de cuatro principios activos: paritaprevir, ritonavir, dasabuvir y ombitasvir).
En concreto, se ha establecido un techo de gasto de 727 millones de euros, a pagar en tres años, lo que garantiza que los servicios de salud puedan asegurar el acceso a estos medicamentos a los pacientes de manera inmediata (el Plan establece un plazo de tres semanas) a los que se los prescriban los hepatólogos en base a los criterios incluidos en el Plan.
Gonzalo A. Amaro Castro
Bibliografía:
Plan de prevención y control de la hepatitis C de la Comunidad Autónoma de Madrid
- Información para pacientes:
- Protocolo de vigilancia y control:
- Protocolo de tratamiento y seguimiento de pacientes:
Agencia Europea de Medicamentos http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002798/WC500160597.pdf
Harrison, principios de medicina interna, 18º ed. Cap 306. Hepatitis crónica viral.
Medimecum, guía de terapia farmacológica, Ed. Adis.
UpToDate. http://www.uptodate.com/es/home.
Agencia española de medicamentos y productos sanitarios (AEMPS). http://www.aemps.gob.es/cima/fichasTecnicas.do?metodo=detalleForm
Ministerio de Sanidad, Servicios Sociales e Igualdad. http://www.msssi.gob.es/gabinete/notasPrensa.do?id=3576
- Cuidados Centrados en el Desarrollo y la Familia (CCD) y NIDCAP
- El Ángel de la misericordia debe morir