Prevenir las complicaciones del catéter venoso central (CVC)
Los catéteres venosos centrales (CVC) son un método invasivo que nos permiten administrar fármacos, nutrición parenteral o extraer muestras de sangre.
Su uso es necesario en unos casos ante la imposibilidad de accesos venosos periféricos o por la utilización de medicación que no se puede administrar de forma segura por una vía periférica.
Desafortunadamente más del 15% de los pacientes con CVC tienen complicaciones asociadas, de las cuales son complicaciones infecciosas 5-26%, complicaciones mecánicas 5-19% y complicaciones trombóticas el 2-26%.
- Complicaciones infecciosas: infección del punto de inserción que se puede extender a lo largo de la superficie del catéter, contaminación del tapón, colonización dentro de la luz del catéter.
- Complicaciones mecánicas: punción de la arteria, hematoma y neumotórax.
- Complicaciones trombóticas: la importancia clínica de la trombosis es una potencial embolia.
Los lugares de inserción de los catéter venoso central (cvc) son en la vena yugular interna, vena subclavia y vena femoral.
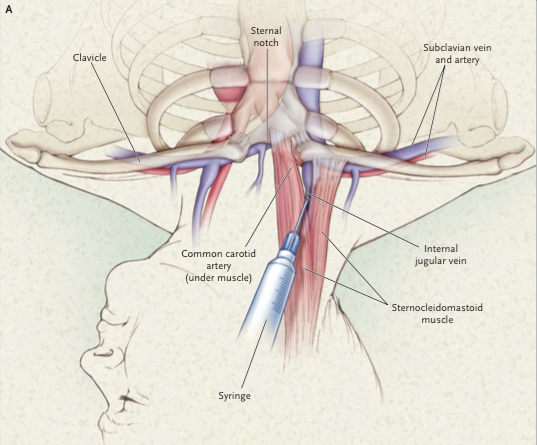
Canalización de un catéter venoso central en la vena yugular interna.
Fuente: McGee DC, Gould MK. Preventing Complications of Central Venous Catheterization. N Engl J Med. 2003 Mar 20;348(12):1123–33.
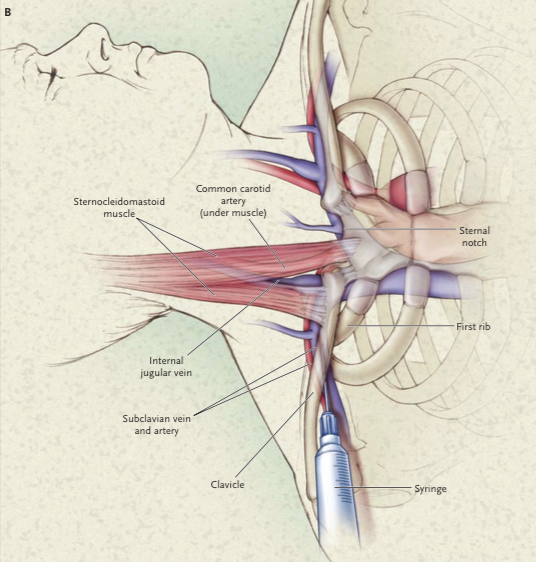
Canalización de un catéter venoso central en la vena subclavia.
Fuente: McGee DC, Gould MK. Preventing Complications of Central Venous Catheterization. N Engl J Med. 2003 Mar 20;348(12):1123–33.
Hay catéteres de una y de varias luces, no hay relación directa entre el número de luces y las complicaciones relacionadas con el catéter(1,2) por lo que la elección dependerá de las necesidades del paciente.
Intervenciones para prevenir las complicaciones por infección.
- El riesgo de infección relacionado con el catéter es menor con los cvc en subclavia frente a los cvc yugular y femoral(3–6).
- Realizar la inserción del catéter garantizando una técnica estéril, el uso de guantes estériles, mascarilla, gorro, bata estéril y paños estériles reduce el porcentaje de infecciones y reduce los costes(7).
- Limpiar la zona preferentemente con soluciones de clorhexidina frente al uso de povidona yodada, la clorhexidina reduce el riesgo de colonización del catéter(8,9).
- Evitar el uso de pomadas antibióticas, se ha comprobado que aumenta el porcentaje de colonización por hongos(10), contribuye al desarrollo de bacterias resistentes a antibióticos(11) y no se ha demostrado que modifique el riesgo de infección(12).
- Desinfectar los tapones de las luces ya que son un lugar frecuente de contaminación(12).
- Programar un cambio de cvc en otro sitio cada cierto tiempo no reduce el riesgo de infección relacionado con el cvc(13,14) y el intercambio de cvc con una guía se asocia a un aumento de las infecciones relacionadas por el catéter(13).
- La probabilidad de colonización del catéter aumenta con el tiempo(4,15,16).
Intervenciones para prevenir las complicaciones mecánicas.
- Reconocer el riesgo de una canalización dificultosa comprobando en la historia clínica la presencia de malformaciones, antecedentes de cirugías que pudieran afectar la anatomía.
- La canalización de cvc por un médico que ha canalizado 50 o más cvc reduce a la mitad la probabilidad de complicaciones mecánicas(17).
- La frecuencia de complicaciones mecánicas en cvc femoral es mayor que en subclavia y yugular(3,17–20), el porcentaje de complicaciones graves es similar entre femoral y subclavia(3).
- El uso de ultrasonidos para guiar la canalización de la vena yugular interna reduce el tiempo de la técnica, reduce el número de punciones fallidas, reduce la probabilidad de punción en la arteria carótida y reduce la probabilidad de formarse un hematoma(21,22).
Intervenciones para prevenir las complicaciones trombóticas.
- El riesgo de trombosis, es menor en los catéteres en subclavia, comparado con femoral y yugular(3,23).
Intervención ante la sospecha de sepsis relacionada con catéter venoso central.
La sepsis se define como una respuesta sistémica en respuesta a una infección, debe cumplir dos o más condiciones
- Temperatura por encima de 38.5ºC o por debajo de 36ºC.
- Frecuencia cardiaca por encima de 90 lpm.
- Frecuencia respiratoria por encima de 20 rpm o PaCO2 por debajo de 32 mmHg.
- Recuento de leucocitos superior a 12000 mm3 o menos de 4000 mm3.
Se extraen hemocultivos de cada luz del cvc y otro periférico es importante rotular los hemocultivos para saber de donde se han extraido.
De forma empírica se inicia tratamiento antibiótico mientras se obtiene algún resultado de los hemocultivos.
Bibliografía.
- Bold RJ, Winchester DJ, Madary AR, Gregurich MA, Mansfield PF. Prospective, randomized trial of Doppler-assisted subclavian vein catheterization. Arch Surg Chic Ill 1960. 1998 Oct;133(10):1089–93.
- Clark-Christoff N, Watters VA, Sparks W, Snyder P, Grant JP. Use of triple-lumen subclavian catheters for administration of total parenteral nutrition. JPEN J Parenter Enteral Nutr. 1992 Oct;16(5):403–7.
- Merrer J, De Jonghe B, Golliot F, Lefrant JY, Raffy B, Barre E, et al. Complications of femoral and subclavian venous catheterization in critically ill patients: a randomized controlled trial. JAMA. 2001 Aug 8;286(6):700–7.
- Raad I, Darouiche R, Dupuis J, Abi-Said D, Gabrielli A, Hachem R, et al. Central venous catheters coated with minocycline and rifampin for the prevention of catheter-related colonization and bloodstream infections. A randomized, double-blind trial. The Texas Medical Center Catheter Study Group. Ann Intern Med. 1997 Aug 15;127(4):267–74.
- Heard SO, Wagle M, Vijayakumar E, McLean S, Brueggemann A, Napolitano LM, et al. Influence of triple-lumen central venous catheters coated with chlorhexidine and silver sulfadiazine on the incidence of catheter-related bacteremia. Arch Intern Med. 1998 Jan 12;158(1):81–7.
- McKinley S, Mackenzie A, Finfer S, Ward R, Penfold J. Incidence and predictors of central venous catheter related infection in intensive care patients. Anaesth Intensive Care. 1999 Apr;27(2):164–9.
- Raad II, Hohn DC, Gilbreath BJ, Suleiman N, Hill LA, Bruso PA, et al. Prevention of central venous catheter-related infections by using maximal sterile barrier precautions during insertion. Infect Control Hosp Epidemiol. 1994 Apr;15(4 Pt 1):231–8.
- Maki DG, Ringer M, Alvarado CJ. Prospective randomised trial of povidone-iodine, alcohol, and chlorhexidine for prevention of infection associated with central venous and arterial catheters. Lancet. 1991 Aug 10;338(8763):339–43.
- Mimoz O, Pieroni L, Lawrence C, Edouard A, Costa Y, Samii K, et al. Prospective, randomized trial of two antiseptic solutions for prevention of central venous or arterial catheter colonization and infection in intensive care unit patients. Crit Care Med. 1996 Nov;24(11):1818–23.
- Flowers RH, Schwenzer KJ, Kopel RF, Fisch MJ, Tucker SI, Farr BM. Efficacy of an attachable subcutaneous cuff for the prevention of intravascular catheter-related infection. A randomized, controlled trial. JAMA. 1989 Feb 10;261(6):878–83.
- Zakrzewska-Bode A, Muytjens HL, Liem KD, Hoogkamp-Korstanje JA. Mupirocin resistance in coagulase-negative staphylococci, after topical prophylaxis for the reduction of colonization of central venous catheters. J Hosp Infect. 1995 Nov;31(3):189–93.
- Maki DG, Band JD. A comparative study of polyantibiotic and iodophor ointments in prevention of vascular catheter-related infection. Am J Med. 1981 Mar;70(3):739–44.
- Cook D, Randolph A, Kernerman P, Cupido C, King D, Soukup C, et al. Central venous catheter replacement strategies: a systematic review of the literature. Crit Care Med. 1997 Aug;25(8):1417–24.
- Bonawitz SC, Hammell EJ, Kirkpatrick JR. Prevention of central venous catheter sepsis: a prospective randomized trial. Am Surg. 1991 Oct;57(10):618–23.
- Maki DG, Stolz SM, Wheeler S, Mermel LA. Prevention of central venous catheter-related bloodstream infection by use of an antiseptic-impregnated catheter. A randomized, controlled trial. Ann Intern Med. 1997 Aug 15;127(4):257–66.
- Collin GR. Decreasing catheter colonization through the use of an antiseptic-impregnated catheter: a continuous quality improvement project. Chest. 1999 Jun;115(6):1632–40.
- Sznajder JI, Zveibil FR, Bitterman H, Weiner P, Bursztein S. Central vein catheterization. Failure and complication rates by three percutaneous approaches. Arch Intern Med. 1986 Feb;146(2):259–61.
- Mansfield PF, Hohn DC, Fornage BD, Gregurich MA, Ota DM. Complications and failures of subclavian-vein catheterization. N Engl J Med. 1994 Dec 29;331(26):1735–8.
- Martin C, Eon B, Auffray JP, Saux P, Gouin F. Axillary or internal jugular central venous catheterization. Crit Care Med. 1990 Apr;18(4):400–2.
- Timsit JF, Bruneel F, Cheval C, Mamzer MF, Garrouste-Orgeas M, Wolff M, et al. Use of tunneled femoral catheters to prevent catheter-related infection. A randomized, controlled trial. Ann Intern Med. 1999 May 4;130(9):729–35.
- Teichgräber UK, Benter T, Gebel M, Manns MP. A sonographically guided technique for central venous access. AJR Am J Roentgenol. 1997 Sep;169(3):731–3.
- Randolph AG, Cook DJ, Gonzales CA, Pribble CG. Ultrasound guidance for placement of central venous catheters: a meta-analysis of the literature. Crit Care Med. 1996 Dec;24(12):2053–8.
- Timsit JF, Farkas JC, Boyer JM, Martin JB, Misset B, Renaud B, et al. Central vein catheter-related thrombosis in intensive care patients: incidence, risks factors, and relationship with catheter-related sepsis. Chest. 1998 Jul;114(1):207–13.
- McGee DC, Gould MK. Preventing Complications of Central Venous Catheterization. N Engl J Med. 2003 Mar 20;348(12):1123–33.
- El segundo sexo coreano. Otras formas de percibir la salud y la enfermedad
- De palabras y funciones. Reflexiones tras una noche de trabajo.

Muy buena información gracias por compartir.
interesante información, gracias por la aportación.