En la entrada de hoy nos centramos en el uso de los diferentes laxantes que podemos encontrar en nuestra unidad de trabajo, exponemos sus propiedades y las diferencias que existen entre ellos.
Si quieres saber más sobre los laxantes que administramos a diario, te animamos a que sigas leyendo, seguro que encontrarás de gran utilidad esta entrada.
Sabrás más sobre: lactulosa, emuliquen, macrogol, puntualex, plantago ovata, enema casen y clisteran.
En términos generales, se habla de estreñimiento cuando sucede disminución de la frecuencia de defecaciones o una reducción del volumen de las heces. Sin embargo, el término se aplica, de forma un tanto imprecisa, a otras situaciones tales como una consistencia pétrea (dura) de las heces. En realidad, no existe una norma fija para determinar cuando existe estreñimiento y, de hecho, la percepción del propio sujeto es fundamental, hay personas que se sienten estreñidas a pesar de que su frecuencia de defecación, la consistencia, peso y volumen de las heces pueden considerarse normales en términos estadísticos. Lo cual incide claramente en el carácter patológico del estreñimiento, se trata de un síntoma más que de una enfermedad.
Color:

Fuente infografía: http://healthnbodytips.com
Las heces suelen presentar un color pardo.
- En el caso de que contengan gran cantidad de pigmentos biliares toman un aspecto más oscuro.
- Una coloración muy oscura, de aspecto similar al alquitrán se suele asociar a la presencia de sangre de procedencia digestiva superior (estómago, duodeno).
- Si la sangre procede de hemorragias presentes en zonas más próximas al recto, las heces toman un color rojizo o abiertamente rojas, con manchas distribuidas de forma no homogénea.
- Durante la lactancia tienen color amarillento, que vira a verdoso por la acción del aire.
- Las heces acólicas presentan color claro o incluso blanco, teniendo en este caso bastante cantidad de grasa no emulsionada.
- En las esteatorreas de origen pancreático aparecen con color amarillo pardo y con aspecto oleoso.
Textura:
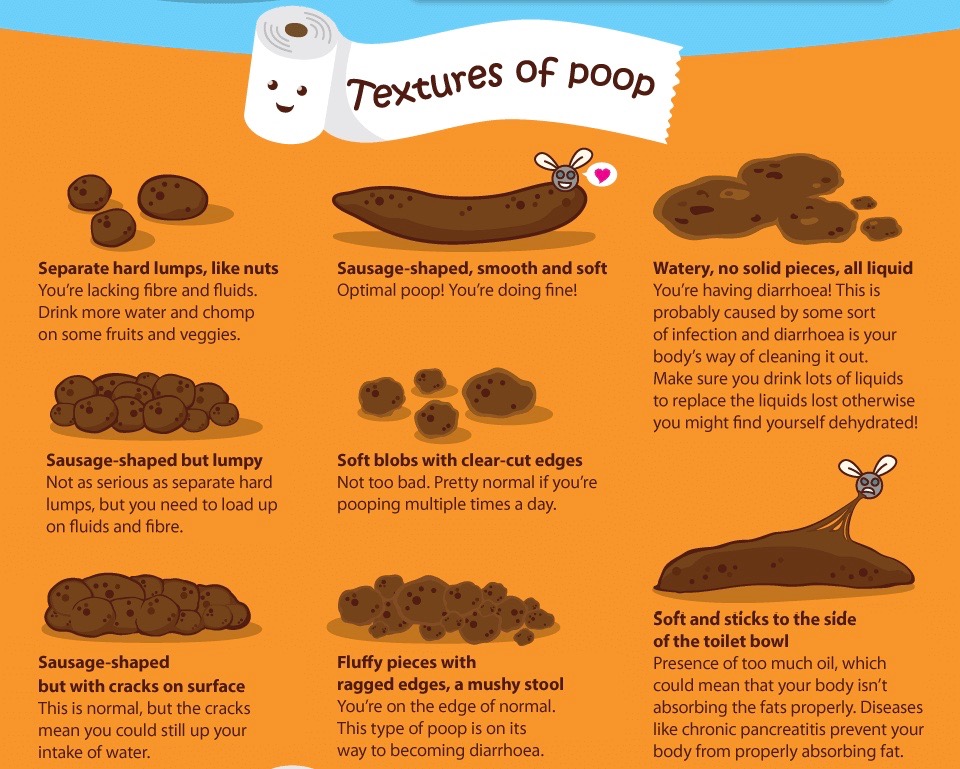
Fuente infografía: http://healthnbodytips.com
Habitualmente son duras y consistentes, aunque en ciertas situaciones puede variar su consistencia.
- Las deposiciones semiblandas indican un tránsito rápido o son propias de afecciones biliares o pancreáticas.
- Son duras en los casos de estreñimiento, presentando forma acintada (aplanadas) en las obstrucciones mecánicas y en forma de grandes bolas en la atonía intestinal. Si son pequeñas y redondeadas son indicativas de estados espásticos acentuados.
- La presencia de sustancias escasamente digeridas o sin digerir es propia de alteraciones en los procesos digestivos, mientras que la aparición de moco o de pus, generalmente se asocia a estados inflamatorios, como colitis o enteritis.
En bastantes ocasiones el estreñimiento se relaciona con la presencia de otros síntomas, entre los que destacan la falta de apetito, la distensión (hinchazón) abdominal, así como malestar general, dolor lumbar y cefalea.
Los medicamentos utilizados para tratar el estreñimiento se agrupan bajo la denominación de laxantes o catárticos, que genéricamente actúan facilitando el tránsito de las heces desde el colon al recto, fomentando la defecación.
El laxante ideal debería no ser irritante ni tóxico, actuar solamente en colon descendente y sigmoideo, y producir heces normales dentro de las siguientes horas, después de las cuales su acción como laxante debería cesar, restaurándose la actividad colónica normal. Obviamente es imposible encontrar un laxante que cumpla todas estas condiciones, Por lo que se suele seleccionar el producto que por su mecanismo de acción resulta más adecuado al tipo de estreñimiento padecido por cada paciente.
- Incrementadores de la masa (bolo) intestinal (plantago ovata).
- Emolientes (suavizantes) y lubrificantes (parafina líquida).
- Agentes osmóticos.
- Derivados de azúcares simples (lactulosa).
- Salinos (enema Casen).
- Polioles (enema glicerina, macrogol)
- Estimulantes de la mucosa intestinal (senósidos A+B).
Incrementadores de la masa:
Son sustancias que ayudan a aumentar la masa de la materia fecal, ya que se hinchan debido a la absorción de agua que experimentan. El incremento del bolo intestinal estimula el peristaltismo, facilitando la evacuación de las heces. Además, inducen el reblandecimiento de las heces, lo que favorece su eliminación. Facilita la deposición de las heces en casos de deposiciones dolorosas, por ejemplo tras cirugía rectal o anal, fisuras anales y hemorroides. Los más empleados son metilcelulosa, agar y semillas de Plantago.
Plantaben contiene cutícula de semillas de Plantago ovata, se presenta en polvo efervescente, de color beige y aroma a naranja, para administración por vía oral, una vez disperso en agua.
Se administra 1 sobre de 2 a 3 veces al día, según necesidad y respuesta.
Para la correcta administración se recomienda vaciar el contenido del sobre en un vaso de agua fría o cualquier otro líquido (200 cc), agitar la mezcla hasta que sea uniforme, y beber inmediatamente. Se recomienda ingerir a continuación otro vaso de líquido.
Puede administrarse antes o después de las comidas. Si se administra antes de las comidas producirá sensación de saciedad.
Se aconseja tomar con 1 ó 2 litros de agua al día. La ingestión de este producto sin la adecuada cantidad de líquido puede originar un bloqueo en la garganta o el esófago.
No se debe tomar el preparado y tumbarse inmediatamente después.
En pacientes diabéticos insulinodependientes puede ser necesario disminuir la dosis de insulina, cuando este medicamento se toma con las comidas.
Emolientes (suavizantes) y lubrificantes:
Se pueden utilizar en aquellos casos en los que interese mantener heces blandas para evitar esfuerzos excesivos, como ocurre en el caso de las hernias, aneurismas, hipertensión, infarto de miocardio, accidente cerebrovascular, cirugía abdominal y anorrectal, etc. Sin embargo, la utilización rutinaria de estos fármacos no es demasiado adecuada por una serie de efectos secundarios, asociados a su uso continuado.

La parafina líquida (emuliquen) es un líquido blanco, con olor a vainilla y sabor dulce.
Se administra 1 sobre en ayunas antes de acostarse, si es necesario, repetir la dosis por la mañana 2 horas antes o después del desayuno, no debe administrarse más de 2 sobres al día.
Antes de abrir el sobre, presionar el sobre con los dedos, en distintas direcciones, para aumentar la fluidez de la emulsión y homogeneizar el contenido.
La dosis a administrar debe ser siempre diluida en un vaso de agua u otro líquido frío o caliente (leche, zumos, etc.).
No debe tomar este medicamento en posición acostada.
Para ayudar a producir heces blandas y para proteger al paciente frente a la deshidratación, cuando se pierde un gran volumen de agua con las deposiciones, es necesario ingerir por lo menos de 6 a 8 vasos de líquido diario.
No debería ser administrado junto con las comidas, puesto que retrasa el vaciado gástrico, aumentando el tiempo de permanencia de los alimentos en el estómago.
Los efectos secundarios más importantes están asociados a su uso repetido y fuertemente ligados a su absorción. Un efecto importante es el relacionado con su aspiración, especialmente en pacientes que se encuentran encamados. En este caso, al ser administrado puede alcanzar la faringe, la tráquea e incluso llegar a los pulmonares, pudiendo originar una neumonía lipídica. Por ello, no se debe administrar reiteradamente a pacientes que se encuentren en cama, a niños, ancianos, o pacientes muy debilitados.
Otro importante efecto al que da lugar es la disminución de la absorción de nutrientes lipídicos, particularmente vitaminas liposolubles como las A, E, D y K.
La concentración de glucosa en sangre puede aumentar tras la administración prolongada de laxantes.
Tratamientos prolongados con Emuliquen Laxante pueden producir tolerancia a la acción laxante y dependencia para conseguir la evacuación.
Agentes osmóticos.
Son aquéllos que producen la atracción de agua a la luz intestinal, actúan creando una fuerte presión osmótica en el recto, de este modo, disminuye la consistencia de las heces, favoreciendo su tránsito y eliminación. Además, como contienen más agua, aumentan su volumen, lo que produce distensión de la luz colónica e incremento del peristaltismo intestinal. Por su composición este grupo lo componen los derivados de azúcares simples, salinos y polioles.
Derivados de azúcares simples.
Entre los más usados la lactulosa.

Se presenta en solución oral de color amarillento, está indicado en las siguientes afecciones:
- Tratamiento del estreñimiento habitual y crónico.
- Ablandamiento de las heces y facilitación de la defecación en pacientes con entidades nosológicas que
afecten al recto y ano, tales como hemorroides, fisura anal, fístulas, abscesos anales, úlceras solitarias y
post-cirugía rectoanal.
- Tratamiento y prevención de la encefalopatía hepática portosistémica.
Dado que lactulosa ejerce su efecto cuando alcanza el colon, pueden transcurrir 1-2 días antes de que se produzca la defecación normal.
La dosis debe ajustarse individualmente, no obstante, la pauta posológica recomendada es la siguiente:
Dosis diaria recomendada al inicio del tratamiento: 30 ml de solución oral, repartida en dos tomas dosis de mantenimiento recomendada: 15-30 ml de solución oral al día, administrada en una sola toma, preferiblemente durante el desayuno. En general, la dosis de inicio puede reducirse a la dosis de mantenimiento a los 2-3 días.
Lactulosa se puede diluir con agua u otro líquido apropiado (zumo de naranja, café, té…).
Para el ablandamiento de las heces y facilitación de la defecación en pacientes con hemorroides, fisura anal, fístulas, abscesos anales, úlceras solitarias y post cirugía recto anal, se administrará un sobre, 1, 2 o 3 veces al día hasta conseguir una consistencia adecuada de las heces.
En caso de encefalopatía portosistémica
la dosis recomendada al inicio del tratamiento es de 2-3 sobres, tres veces al
día.
La dosis de mantenimiento se fijará con el fin de conseguir un máximo de 2-3 deposiciones de consistencia semisólida al día.
En el caso de emplear dosis altas superiores a las recomendadas (mayores de 3 sobres al día), es preciso tener en cuenta la presencia de azúcares en la composición del medicamento.
Este medicamento contiene lactosa, galactosa y fructosa. Los pacientes con intolerancia no deben tomar este medicamento.
Durante los primeros días de tratamiento puede producirse meteorismo y flatulencia que, generalmente, desaparece con la terapia continuada.
Especialmente con dosis elevadas, puede producirse dolor abdominal y diarrea con sus potenciales complicaciones: depleción de líquidos, hipopotasemia e hipernatremia.
Lactulosa puede administrarse en enema para paciente en los que es necesaria una acción más rápida, la composición recomendada es de 300 ml de lactulosa diluidos en 700 ml de agua. El enema se retendrá unos 30/60 minutos.
Salinos.
Enema Casen solución rectal incolora e inodora que se presenta en envases de 250 ml, 140 ml y 80 ml de plástico flexible, herméticamente cerrados, con válvula antiretorno y una cánula rectal prelubricada exenta de látex. Su uso está indicado en aquellos casos en que sea necesaria una evacuación intestinal, tales como:
- Pre y post cirugía.
- Parto y post parto.
- Antes de rectoscopia, sigmoidoscopia y colonoscopia.
- Antes de exámenes radiológicos.
- Impactación fecal.
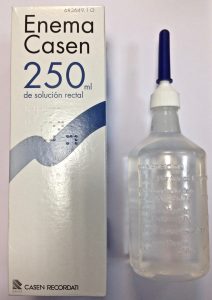
La dosis recomendada es de un único enema de 140 mL ó 250 mL. Se podrá administrar una vez al día, durante un máximo de 6 días consecutivos.
Enema casen se administra por vía rectal y debe administrarse a temperatura ambiente.
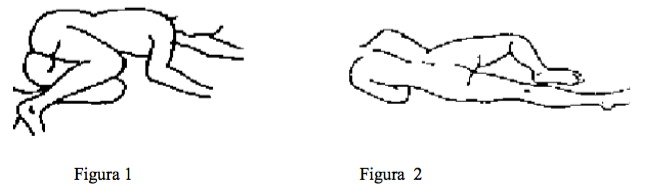
Para la aplicación del enema casen se recomienda que el paciente esté reclinado sobre el lado izquierdo y con ambas piernas dobladas sobre el pecho (Figura 1) o reclinado con la pierna izquierda extendida y la derecha doblada sobre el pecho (Figura 2).
Para administrar el enema quitamos la funda protectora azul de la cánula prelubricada, introdúzcase la cánula en el recto de forma cuidadosa para evitar lesionar la pared del mismo y oprímase el envase, de manera suave y continuada, hasta que penetre la cantidad de líquido requerida. Conviene que el paciente mantenga dicha posición hasta que sienta fuertes deseos de defecar.
Generalmente, de 2 a 5 minutos son suficientes para obtener el efecto deseado.
Está contraindicado su uso en pacientes con ileostomía.
Los enemas nunca deben ser considerados como una alternativa cómoda, eficaz y segura a los laxantes convencionales, ya que su uso habitual puede reducir drásticamente el funcionalismo intestinal.
Cuando se administran por vía rectal, como enemas, las sales de sodio (como el fosfato sódico) pueden absorberse hasta un 10%, lo que representa un grave inconveniente ya que su uso habitual puede reducir drásticamente el funcionalismo intestinal.
En base a los resultados de estudios clínicos recientes, se ha establecido una relación entre el tiempo de retención del enema casen y un aumento del riesgo de hiperfosfatemia, por lo que no se recomiendan tiempos de retención superiores a 5 minutos.
En caso de sangrado rectal tras la administración de Enema Casen puede indicar una situación grave. En tal caso, se deberá interrumpir la administración inmediatamente y la situación del paciente debe ser valorada por el médico.
Polioles.
Los polietilenglicoles o PEG (macrogoles) de alto peso molecular son grandes cadenas lineales poliméricas (el número que acompaña al macrogol se refiere al peso molecular del compuesto, generalmente entre 3.000 y 4.000 para su uso como laxante), sobre las cuales se fija el agua a través de enlaces por puente de hidrógeno. No se absorben ni se metabolizan y, administrados por vía oral, incrementan el volumen de los líquidos intestinales no absorbidos.
Favorece el peristaltismo y mejora la consistencia de las heces facilitando la evacuación.
A diferencias de los derivados de azúcares simples, los macrogoles no fermentan a nivel intestinal y, por tanto, no generan gases, lo que permite un mejor ajuste de la dosis sin aumento de la flatulencia. Se considera a los macrogoles como un tratamiento seguro y eficaz para el estreñimiento, incluso en niños y pacientes de edad avanzada.

La glicerina o glicerol, generalmente se administra por vía rectal , en forma de supositorios, lo que conduce a un efecto laxante adicional, debido a la irritación local que produce un estímulo nervioso del reflejo de defecación en el recto. En definitiva, su efecto evacuante es debido a la combinación de la actividad higroscópica propia de la glicerina, que hace atraer agua hacia la zona rectal, con lo cual aumenta el volumen de las heces, y al ligero efecto irritante local tanto del estearato sódico (excipiente utilizado habitualmente en los supositorios de glicerina) como de la propia glicerina, que favorece el estímulo reflejo de la defecación.
Se utiliza como laxante de carácter general y la acción tarda entre 15 y 30 minutos en desarrollarse.

En el mercado hay preparados que asocian varios laxantes rectales con glicerol, entre ellos destaca clisteran.
Clisteran es un preparado de laxantes para la administración por vía rectal, actúa como un laxante de tipo osmótico, debido a la acción combinada del citrato trisódico dihidratado, que actúa reteniendo líquido por ósmosis en el intestino, por lo que incrementa el volumen de agua en las heces, y del Laurilsulfoacetato de sodio, un agente humectante.
Antes de introducir la cánula en el recto, debe quitarse el capuchón que cierra el extremo del envase monodosis, ponerlo en posición vertical y presionar el envase hasta que salgan unas gotas de solución para facilitar su introducción en el recto.
Introducir suave y lentamente la cánula en el recto, con el extremo apuntando hacia el ombligo. En caso de encontrar resistencia en el momento de la aplicación, debe interrumpirse la misma ya que puede resultar perjudicial y dañina.
Apretar el envase para vaciar la totalidad del contenido y retirarlo suavemente manteniéndolo presionado.
La absorción de los principios activos por la vía rectal es prácticamente nula.
Estimulantes de la mucosa intestinal.
Actúan estimulando los movimientos intestinales (peristaltismo) por acción directa sobre las terminaciones nerviosas del intestino y por la inhibición de la absorción de electrolitos y agua desde la luz intestinal, produciendo un incremento notable de líquido intestinal que actúa estimulando el peristaltismo. Complementariamente, también actúan adicionalmente estimulando la secreción de agua en el intestino delgado o intestino grueso.
Los senósidos A y B pertenecen a este grupo, su efecto es proporcional a las dosis administradas, obteniendo una respuesta rápida e intensa, en 6-12 horas.
Los mayores riesgos del uso de este tipo de estimulantes están relacionados con pérdidas excesivas de líquidos y electrolitos, pérdida intestinal de proteínas, hipocalcemia y mala absorción debida a la excesiva hipermotilidad.
Los laxantes de tipo estimulante sólo deben utilizarse en caso de que no se consiga el efecto laxante con una dieta rica en fibras vegetales y líquido o tras la administración de agentes incrementadores del bolo fecal.
Cuando se utilicen para lograr el vaciado gastrointestinal, se recomienda administrar la dosis de un frasco de 5 ml en una sola toma. El medicamento debe administrarse el día anterior al examen radiológico, después de la comida del mediodía, que deberá ser ligera y sin contenido en grasa. Una vez ingerido el medicamento, no deberán tomarse alimentos sólidos, y a partir de las 22:00 horas del día previo, tampoco deberán tomarse líquidos.
Bibliografía: